Regards sur le Forum « 3D Planning and Printing in Hospitals » de Materialise, 8ᵉ édition
Aaron James a perdu la moitié de son visage après avoir été électrocuté sur son lieu de travail. Personne ne souhaiterait cela à quiconque. Lorsque Koen Peters, Vice-Président Exécutif de l’unité Médicale de Materialise, a ouvert la 8ᵉ édition du Forum 3D Printing in Hospitals avec l’histoire d’Aaron, le silence s’est fait dans la salle — un silence de reconnaissance.
Nous avions couvert l’opération historique d’Aaron à l’époque, une première mondiale au cours de laquelle les instruments de découpe imprimés en 3D par Materialise ont aidé les chirurgiens à réaliser une greffe totale du visage et de l’œil. Aujourd’hui, Aaron va bien. Il a retrouvé une forme de normalité. Il est la preuve vivante de ce qui devient possible lorsque technologie, planification et précision chirurgicale convergent autour de l’anatomie d’un seul patient.
C’est l’une de ces histoires que j’aime appeler « miracles médicaux ». C’est aussi, de l’aveu même de Peters, un modèle qui n’est pas viable pour l’avenir des soins de santé.

« La valeur pour les patients est presque évidente, a observé Koen Peters. « Mais le langage que parlent les autorités et les organismes de remboursement, c’est le langage des chiffres. C’est le travail que nous devons vraiment accomplir : démontrer la valeur de manière structurée, en s’appuyant sur des données. »
Ne vous méprenez pas : je ne dis pas que les cas exceptionnels comme celui d’Aaron n’ont pas d’importance. Ils en ont, profondément. Mais s’il est une chose que j’ai retenue de ma participation à la conférence de Materialise, c’est que l’adoption de la technologie 3D dans les hôpitaux ne peut pas se construire sur des réussites isolées.
Elle nécessite des systèmes, des flux de travail, des résultats reproductibles, et surtout, une planification quotidienne qui ne fait jamais la une des journaux.
Un a priori qui a forgé le discours du secteur sur la technologie 3D en santé
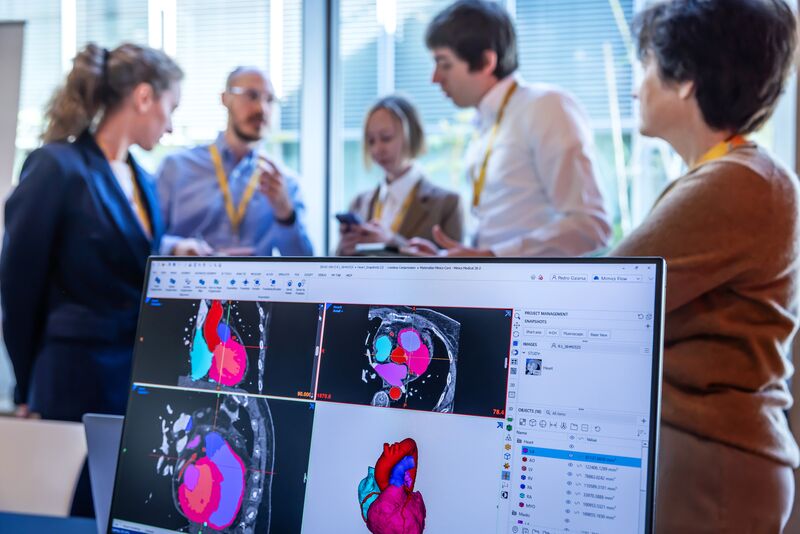 Il existe un a priori qui a forgé la manière dont une grande partie du secteur parle de la technologie 3D dans la santé et en tant que publication spécialisée, nous avons certainement contribué à placer l’impression 3D sur ce piédestal. L’idée reçue est que l’objectif final est toujours l’impression 3D. Ce n’est pas le cas. Ou du moins, ce n’est pas toujours le cas. Et ce forum l’a clairement établi.
Il existe un a priori qui a forgé la manière dont une grande partie du secteur parle de la technologie 3D dans la santé et en tant que publication spécialisée, nous avons certainement contribué à placer l’impression 3D sur ce piédestal. L’idée reçue est que l’objectif final est toujours l’impression 3D. Ce n’est pas le cas. Ou du moins, ce n’est pas toujours le cas. Et ce forum l’a clairement établi.
Dans toutes les spécialités (chirurgie craniomaxillofaciale, oncologie, cardiologie, urologie, orthopédie et pédiatrie) les intervenants, les uns après les autres, ont décrit comment la planification 3D seule avait transformé ce qui se passe en salle d’opération. Parce qu’ils pouvaient voir l’anatomie avant de pratiquer la première incision.
Un chiffre présenté lors du forum a particulièrement retenu l’attention : les modèles 3D ont modifié le plan chirurgical dans 44 % des cas impliquant des cardiopathies congénitales. Près de la moitié. Ce qui signifie que, sans le modèle 3D, près de la moitié de ces approches chirurgicales auraient été basées sur un tableau incomplet.
Considérons ce que cela implique en pratique. Dans un cas oncologique complexe — une reconstruction mandibulaire à partir de segments de fibula, par exemple —, la planification géométrique de ces segments osseux dans un logiciel peut réduire une intervention qui prendrait autrement des heures d’improvisation à une séquence pré-établie de 5 à 10 minutes.
Comme me l’a expliqué Arsham Makaryan, ingénieur applicatif chez Materialise, lors d’une démonstration logicielle : chaque minute économisée en salle d’opération, c’est le temps de 10 à 15 personnes économisé simultanément. « Toute la planification, toute la pré-planification que vous pouvez faire avant la chirurgie permet d’économiser le temps de ces personnes en même temps. »
Ce que les applications cliniques nous enseignent réellement
 La diversité des cas d’usage présentés lors du forum de cette année témoigne de l’étendue de la diffusion du 3D au point de soin bien au-delà de ses bastions d’origine que sont la chirurgie craniomaxillofaciale et l’orthopédie.
La diversité des cas d’usage présentés lors du forum de cette année témoigne de l’étendue de la diffusion du 3D au point de soin bien au-delà de ses bastions d’origine que sont la chirurgie craniomaxillofaciale et l’orthopédie.
En cardiologie, le cardiologue Joan Sanchez-de-Toledo a expliqué comment les modèles 3D des cardiopathies congénitales, notamment les anatomies pédiatriques complexes, ont transformé la fois la préparation chirurgicale et la communication avec les familles. Le même modèle qui aide un chirurgien à comprendre où intervenir aide un parent à comprendre ce que vit son enfant. Le logiciel, a-t-il souligné, offre aux équipes la possibilité de s’adapter au patient : à la famille, au chirurgien, à l’anatomie spécifique.
En oncologie et chirurgie reconstructrice, le forum a mis en lumière la manière dont la planification virtuelle pour la reconstruction mandibulaire, où les chirurgiens assemblent des sections réséquées de la mâchoire à l’aide de segments de fibula est devenue réalisable et efficace. Ce qui exigeait autrefois improvisation et pression en salle opératoire dispose désormais d’une feuille de route.
En chirurgie générale et urologique, des équipes d’institutions dont l’eDIMES Lab ont présenté comment la planification préopératoire et la navigation peropératoire sont appliquées dans les interventions vasculaires, gynécologiques et urologiques, des domaines où la planification 3D progresse encore.
En chirurgie CMF et orbitaire, un laboratoire 3D au point de soin a montré comment la planification conventionnelle avait historiquement généré des déviations d’implants allant jusqu’à 40 degrés. Avec les approches guidées par la 3D et la navigation peropératoire en temps réel, ces marges ont été considérablement réduites. L’avenir qu’ils construisent, ont-ils souligné, inclut l’IA, la réalité augmentée et la robotique.
Mimics: le fil conducteur de toutes ces applications
Présente en filigrane dans presque toutes les applications cliniques présentées lors du forum, la plateforme logicielle Mimics de Materialise constitue l’infrastructure par laquelle les scanners CT deviennent des anatomies 3D navigables, et les anatomies se transforment en plans chirurgicaux.
Mimics s’appréhende avant tout comme un écosystème logiciel. En son cœur se trouve Mimics Core, la boîte à outils d’ingénierie complète permettant aux utilisateurs de segmenter les données CT et IRM, de générer des modèles de surface de n’importe quelle structure anatomique, et d’effectuer des mesures, de concevoir des guides chirurgicaux ou de simuler des procédures. Il est utilisé par des ingénieurs biomédicaux, des ingénieurs cliniques et un nombre croissant de chirurgiens directement.
Le processus de segmentation qui consiste en convertir les coupes 2D empilées d’un scanner CT en modèle 3D manipulable est plus subtil qu’il n’y paraît. Différents tissus possèdent différentes valeurs de radiodensité ; le bon seuil détermine si l’on visualise un cœur ou une cage thoracique. Comme l’a démontré Arsham Makaryan, ingénieur applicatif chez Materialise : « C’est à moi de choisir le bon seuil. Tout se résume à cela. »
À partir de ce modèle, le logiciel permet aux utilisateurs d’isoler, nettoyer, coder par couleur, mesurer et exporter n’importe quelle structure d’intérêt.
Certaines segmentations, notamment celles impliquant des données IRM ou des cas oncologiques des tissus mous, peuvent prendre deux heures ou plus. D’autres s’achèvent en quelques minutes. Le logiciel s’adapte au cas.
Aux côtés de Mimics Core, on trouve un portefeuille de planificateurs spécifiques à chaque spécialité, dont Mimics Enlight CMF, conçu pour les chirurgies orthognathiques, traumatologiques et de reconstruction impliquant résection, reconstruction basée sur la fibula et la scapula. Ces planificateurs sont conçus pour être utilisés directement par les cliniciens. Lors d’une démonstration d’Enlight CMF, les étapes allant de la mise en miroir d’une mandibule saine à la planification de trois placements de segments osseux ont pris moins de dix minutes, grâce à l’environnement de planification que la solution logicielle permet.
 « Nous appelons Mimics une boîte à outils », a expliqué Beatriz Domínguez González, Responsable de Marché Logiciels pour les Hôpitaux et Universités. « Vous l’ouvrez, et selon ce que vous devez faire ce jour-là, vous choisissez vos outils. Nous disposons également de planificateurs anatomiques spécifiques où nous sommes allés de plus en plus loin dans la précision. Ces outils logiciels sont très performants pour réaliser une tâche spécifique, et ils rendent la chose aussi simple que possible pour que les chirurgiens puissent les utiliser eux-mêmes. »
« Nous appelons Mimics une boîte à outils », a expliqué Beatriz Domínguez González, Responsable de Marché Logiciels pour les Hôpitaux et Universités. « Vous l’ouvrez, et selon ce que vous devez faire ce jour-là, vous choisissez vos outils. Nous disposons également de planificateurs anatomiques spécifiques où nous sommes allés de plus en plus loin dans la précision. Ces outils logiciels sont très performants pour réaliser une tâche spécifique, et ils rendent la chose aussi simple que possible pour que les chirurgiens puissent les utiliser eux-mêmes. »
La question de savoir qui utilise le logiciel — ingénieur ou chirurgien — s’avère moins « binaire » qu’attendu. González a souligné que si les ingénieurs gèrent la segmentation technique dans la plupart des hôpitaux, de nombreux cliniciens sont capables d’utiliser les outils directement, les récents progrès les ayant rendus beaucoup plus accessibles, notamment au sein des interfaces de planificateurs guidés. « C’est davantage une question de temps, dans certains cas. Un médecin dispose d’un temps limité. Il préfère donc qu’un ingénieur réalise l’essentiel du travail de segmentation pour pouvoir se concentrer sur la planification chirurgicale. Mais il pourrait le faire lui-même. »
L’avancée clé de la planification 3D, a-t-elle souligné, réside dans la modélisation de surface, par opposition au rendu volumique. Pour les anatomies complexes comme les cœurs congénitaux, la segmentation basée sur les surfaces est la seule approche qui atteint la précision nécessaire. Et les capacités de conception CAO superposées permettent aux équipes de passer de l’anatomie à la conception de guides physiques au sein d’une même plateforme. « Nous avons cette combinaison », a-t-elle dit : le diagnostic et la conception, dans un même environnement.
Où se situe vraiment l’obstacle?
 « Je pense que c’est davantage du côté opérationnel », argumente González. « C’est intégré dans la planification chirurgicale. Finalement, nous apportons une nouvelle technologie, et cela prend du temps. »
« Je pense que c’est davantage du côté opérationnel », argumente González. « C’est intégré dans la planification chirurgicale. Finalement, nous apportons une nouvelle technologie, et cela prend du temps. »
Le schéma qu’elle a décrit est reconnaissable : un chirurgien voit un collègue utiliser une technologie, demande ce que c’est, l’essaie, et ne veut plus s’en passer. L’adoption se propage latéralement, cas par cas, spécialité par spécialité. La technologie convainc ceux qui la rencontrent. Le défi est de créer suffisamment de rencontres.
Le remboursement est l’autre élément clé. Aux États-Unis, un nouveau code procédural pour la planification chirurgicale virtuelle doit entrer en vigueur en juillet 2026, première reconnaissance formelle de la planification 3D comme activité clinique à part entière. Koen a mesuré ses mots dans son évaluation : « Cela contribue à donner à la planification 3D sa place dans le système. Mais l’étape suivante concerne l’impact au niveau des remboursements, là où se situerait le véritable impact financier majeur. Je ne pense pas que nous en soyons encore là. »
En Europe, la situation est plus fragmentée. L’Espagne a introduit des codes pour la planification virtuelle. Les Pays-Bas disposent d’un consortium d’une vingtaine d’hôpitaux travaillant conjointement avec les autorités sanitaires. L’Islande a un système de remboursement en place depuis des années, même si les volumes restent faibles. González a décrit l’effort européen comme un défi de coordination à long terme : standardiser les preuves entre les systèmes nationaux pour que ce qui est démontré dans un pays puisse appuyer le dossier dans un autre.
« Si j’obtiens le remboursement en Europe », a-t-elle dit, non sans humour, « je pourrai prendre ma retraite mentalement. C’est une mission de vie pour moi : m’assurer que chaque patient qui a besoin de cette technologie puisse y accéder, quel que soit son code postal. »
Koen a ajouté une observation structurelle à retenir : aux États-Unis, deux spécialités (la radiologie et la cardiologie pédiatrique) sont les principaux moteurs de l’adoption, ce qui crée une dynamique commerciale mais aussi une concentration. En Europe, l’adoption est plus distribuée entre les spécialités, comme en témoignent les applications cliniques présentées au forum. Cela génère une diversité d’applications, mais rend le plaidoyer coordonné plus difficile.
Faire de l’exceptionnel une norme de soins
 Le thème choisi par Materialise pour le forum de cette année, « La prédictabilité érigée en routine. Des soins améliorés », souligne le long chemin qui reste à parcourir.
Le thème choisi par Materialise pour le forum de cette année, « La prédictabilité érigée en routine. Des soins améliorés », souligne le long chemin qui reste à parcourir.
Aaron James est vivant, il va bien, il a retrouvé une forme de normalité. Son cas est extraordinaire. Aujourd’hui, Materialise et les cliniciens présents à ce forum œuvrent vers un avenir (ou devrais-je dire un présent) dans lequel les outils qui ont rendu ses soins possibles soient accessibles, de manière systématique, fiable et rentable, à tout patient qui en a besoin.
Comme l’a dit Peters : « Nous nous aventurons toujours en territoire inconnu. C’est inscrit dans notre ADN. Mais la valeur est évidente. Le travail consiste à la démontrer de manière structurée, basée sur des données, dans le langage que les décideurs comprennent. »
Si on lui demande ce qu’il changerait en priorité, la réponse de Peters a été immédiate : « Accélérer cette démonstration de valeur (la valeur que nous apportons manifestement) dans le langage de ceux qui prennent les décisions. Pour les patients. » Une liste de vœux à un seul élément, mais sans doute le plus important à l’ordre du jour dans ce domaine.
Pour les hôpitaux qui envisagent d’investir dans des capacités de planification 3D, le message de ce forum était cohérent : la technologie est prête. Les flux de travail existent. L’argumentaire économique, en termes de seule efficacité opérationnelle, est de plus en plus bien étayé. Et les résultats cliniques — de la reconstruction orbitaire à la chirurgie mandibulaire en passant par la cardiologie congénitale — parlent d’eux-mêmes.
Le travail qui reste à accomplir concerne toujours l’adoption, l’intégration et l’accumulation patiente de preuves qui transforment une étude de cas impressionnante en norme de soins. C’est plus lent, plus difficile, moins photogénique qu’une chirurgie mondiale mais c’est ainsi que la médecine avance réellement.